Les médicaments radiopharmaceutiques
Mis à jour le 17/01/2023
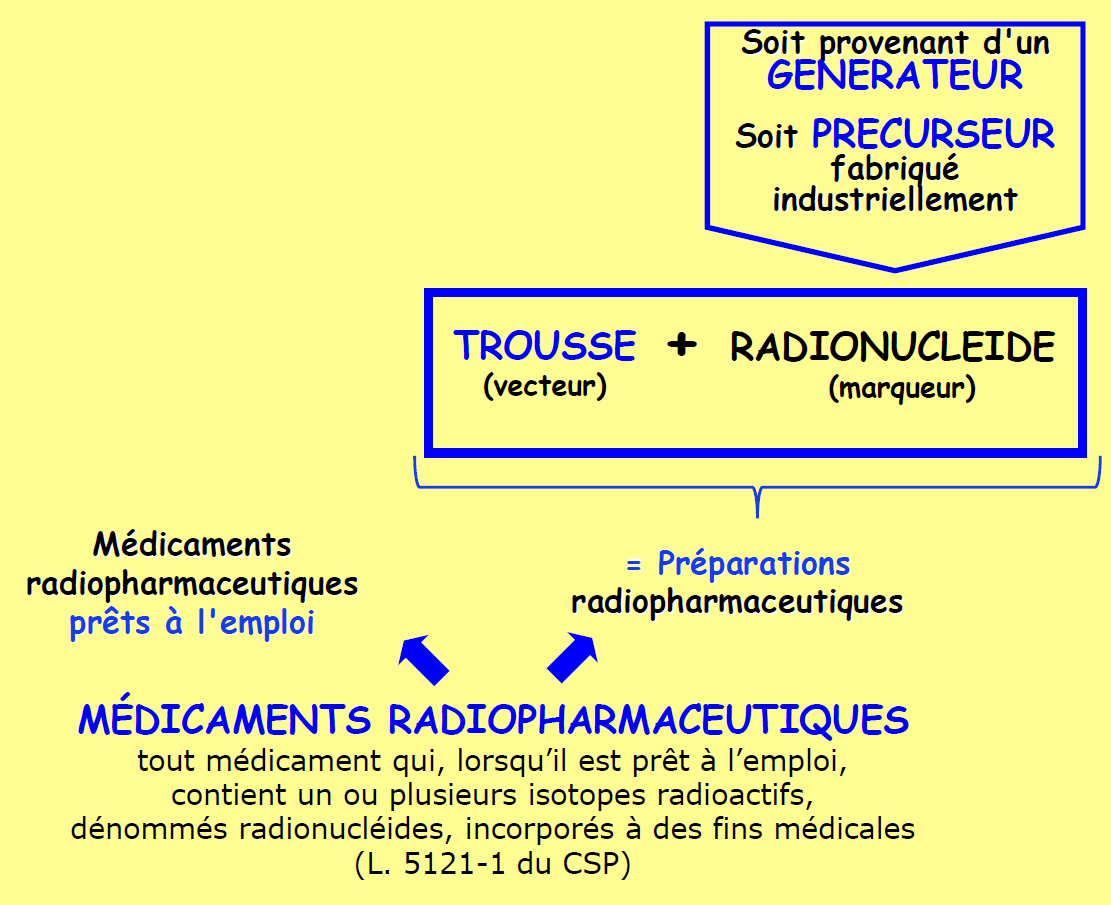
La définition du médicament radiopharmaceutique (MRP) est donnée dans l’article L.5121-1 du Code de la santé publique. Il s’agit de tout médicament contenant un ou plusieurs radionucléides incorporés à des fins médicales.
Les MRP peuvent être utilisés à des fins diagnostiques (scintigraphie et tomographie par émission de positon (TEP)) ou thérapeutiques (radiothérapie interne vectorisée).
Les MRP appartiennent tous à la liste I, certains sont des médicaments dérivés du sang ou sont inscrits sur la liste des médicaments remboursés en sus du groupe homogène de séjours (GHS), avec pour corollaire une obligation de traçabilité.
Les MRP sont majoritairement administrés par voie parentérale. Ils peuvent se présenter soit sous forme d’une spécialité radiopharmaceutique prête à l’emploi, fabriquée par l’industrie pharmaceutique, soit sous forme d’une préparation radiopharmaceutique (PRP) réalisée in situ dans la radiopharmacie.
Les préparations radiopharmaceutiques stériles obtenues sont généralement multidoses, impliquant un respect strict des règles d’asepsie, en plus des règles de radioprotection relatives à la manipulation de sources radioactives non scellées.
La préparation des MRP met en jeu deux catégories de matières premières : le radionucléide (le marqueur) et la trousse (molécule vectrice).
Le radionucléide peut provenir d’un générateur. C’est le cas du technétium 99m (99mTc), radionucléide majoritairement utilisé, qui est obtenu par élution du générateur de 99Mo/99mTc au sein de l’unité de radiopharmacie. Le radionucléide peut également être produit dans un réacteur nucléaire ou un cyclotron puis qualifié industriellement (il porte alors le nom de précurseur) et être livré sous forme de solution stérile prête à l’emploi pour le radiomarquage de molécules vectrices.
La trousse est constituée de molécules ayant un rôle de vecteur et d’excipients, donnant après marquage par le radionucléide approprié le MRP souhaité. Le radiomarquage des molécules vectrices par des atomes de 99mTc nécessite une étape préalable de réduction des atomes de 99mTc qui ensuite pourront se lier aux molécules vectrices.
Quels locaux et équipements ?
Les bonnes pratiques de préparation, récemment mises à jour en septembre 2023, précisent, dans un chapitre dédié, les règles applicables à la préparation de médicaments radiopharmaceutiques.
Les locaux techniques d’une unité de radiopharmacie comprennent généralement un local de livraison, un local destiné à la préparation aseptique en système clos des MRP, avec sas d’accès, si nécessaire un local destiné à la préparation aseptique en système ouvert des MRP (cas notamment les marquages cellulaires radioisotopiques), avec sas d’accès, un local destiné au contrôle de la qualité des produits radiopharmaceutiques et un local destiné au stockage des déchets radioactifs.
Leur aménagement doit répondre aux réglementations en vigueur du point de vue pharmaceutique (zone d’atmosphère contrôlée dont les qualités microbiologiques et particulaires sont maîtrisées), du point de vue de la manipulation de sources radioactives non scellées (zone contrôlée), et des contrôles d’accès dans le but de protéger le personnel et l’environnement.
La préparation des MRP et des doses à administrer est réalisée dans des enceintes blindées et ventilées en dépression. Le blindage de ces équipements et du matériel de radioprotection doit être adapté aux activités, aux types et à l’énergie des rayonnements émis par les radionucléides utilisés.
Quel est le nouveau régime d’autorisation d’activité de médecine nucléaire ?
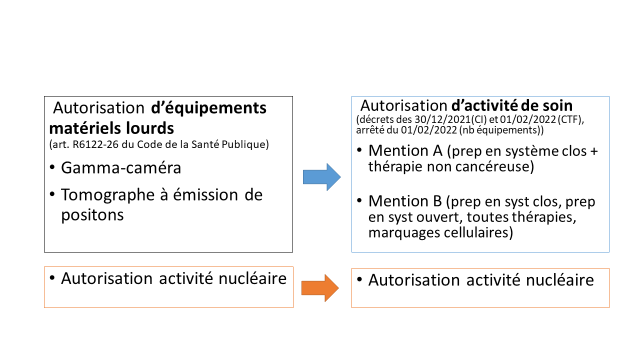
Depuis le décret du 30 décembre 2021, L’activité de médecine nucléaire est désormais classée en mention A ou B selon son niveau de risque basé d’une part sur le type dactivité clinique et d’autre part sur le type de produit pharmaceutique administré .
La classification basée sur l’activité clinique
En mention « A », peuvent être réalisés les actes suivants : actes diagnostiques ou thérapeutiques hors thérapie des pathologies cancéreuses.
En mention « B », outre les actes de la mention A, peuvent être réalisés les actes suivants :
-Les actes diagnostiques réalisés dans le cadre d'explorations de marquage cellulaire des éléments figurés du sang par un ou des radionucléides ;
-les actes thérapeutiques réalisés par l'administration de dispositif médical implantable actif ;
-Les actes thérapeutiques pour les pathologies cancéreuses réalisés par l'administration de médicament radiopharmaceutique.
La classification basée sur le type de produit pharmaceutique engagé
En mention « A », les actes peuvent être réalisés uniquement avec des médicaments radiopharmaceutiques, prêts à l'emploi ou préparés conformément au résumé des caractéristiques du produit, selon un procédé aseptique en système clos.
En mention « B », outre les médicaments mentionnés en « A », les actes cités peuvent être réalisés avec des médicaments radiopharmaceutiques préparés selon un procédé aseptique en système ouvert, ou avec un marquage cellulaire des éléments figurés du sang par un ou des radionucléides, ou avec un dispositif médical implantable actif
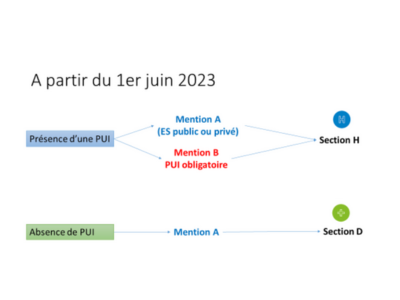
Selon le décret du 1er février 2022, les sites de médecine nucléaire en mention B doivent avoir obligatoirement une PUI, détenant une autorisation d’activité à risque dans le domaine de la radiopharmacie (article R 5126-33 du CSP).
Les sites de médecine nucléaire en mention A, qui correspondent notamment aux centres libéraux de médecine nucléaire, ne disposent pas d’une PUI, mais doivent s'assurer le concours d’un radiopharmacien.
Questions / Réponses
Quelles sont les indications des MRP ?
Les MRP sont majoritairement utilisés pour la réalisation de scintigraphies et de TEP (tomographies par émission de positons) en permettant des explorations morphologiques et fonctionnelles de divers organes ou tissus (en oncologie, cardiologie, endocrinologie, pneumologie, neurologie, néphrologie, etc.). D’autres sont indiqués en thérapie, notamment dans le traitement par l’Iode 131 des pathologies thyroïdiennes (hyperthyroïdie, cancer).
Depuis quelques années, les radiopharmaciens ont à gérer de nouveaux MRP composés d’émetteurs de positons qui ont comme caractéristiques principales d’avoir des périodes physiques relativement courtes (de quelques secondes à 110 minutes selon le radionucléide) et d’émettre des rayonnements dont l’énergie émise après interaction implique la mise en œuvre de mesures de radioprotection particulières. Actuellement, ces MRP sont majoritairement utilisés en onco-hématologie dans le cadre de la tomographie d’émission de positons couplée à la tomodensitométrie (TEP-TDM).
La théranostique en médecine nucléaire consiste à associer un examen diagnostique qui étudie de façon individualisée l'activité tumorale chez le patient et une thérapie ciblée adaptée à sa pathologie cancéreuse. Idéalement, ce sont les mêmes molécules vectrices qui sont mises en jeu. Leur utilisation pour le diagnostic ou la thérapie repose sur la nature des atomes radioactifs qui seront fixés sur ces molécules vectrices. La préparation de MRP de thérapie ciblée est en plein essor.
Liens utiles
- Bonnes pratiques de préparation, chapitre IX : préparations de médicaments radiopharmaceutiques - BO spécial 2007-7bis
- Institut de radioprotection et de sûreté nucléaire
- Autorité de Sûreté Nucléaire
- Arrêté du 16 janvier 2015 portant homologation de la décision n° 2014-DC-0463 de l'Autorité de sûreté nucléaire du 23 octobre 2014 relative aux règles techniques minimales de conception, d'exploitation et de maintenance auxquelles doivent répondre les installations de médecine nucléaire in vivo
- Arrêté du 1er décembre 2003 relatif aux qualifications et à la formation des pharmaciens utilisant des médicaments radiopharmaceutiques dans les établissements de santé et les syndicats interhospitaliers
- Décret n° 2021-1930 du 30 décembre 2021 relatif aux conditions d'implantation de l'activité de médecine nucléaire